ジェンマブがなぜ注目されているか?
このバイオ株について、広瀬さんがコメントした経緯はありませんが、Investor’s Business Dailyでは、 IBD50トップ10リストに追加され、注目されています。新興バイオ企業ではありますが、パイプラインが豊富で今後の成長がかなり期待されます。
Yahoo!financeを参考に編集
ジェンマブ(GMAB)に関するまとめ
主力製品
ジェンマブの主力製品は、多発性骨髄腫薬のダラザレックス(ダラツムマブ)です。2022年9月期(第3四半期)の主力3薬の売上高は以下のとおり。
- DARZALEX®(多発性骨髄腫薬):DKK 3,049M(前年同期比成長率:+68.7%)
- TEPEZZA ®(甲状腺眼疾患薬):DKK 3,049M(前年同期比成長率:-6.8%)
- Kesimpta®(再発性多発性硬化症薬):DKK 213M(前年同期比成長率:+213.2%)
「DARZALEX ®」として販売されているダラツムマブは、市場に出回った最初のヒト CD38 モノクローナル抗体です。ダラツムマブを使用したお薬は、点滴で投与する「DARZALEX®」または注射投与する「DARZALEX SC」があります。

「よく効く薬」として知られ確実に売上高を伸ばしています。日本でもダラツムマブが保険適用され、今後も売上を拡大させるのではないかと期待しています。
「Kesimpta®」(オファツムマブ)は、成人の再発性多発性硬化症 (RMS) の治療薬です。米国、EU、カナダ、日本などで承認されています。進行性多巣性白質脳症(PML)が起こりにくいといわれ、安全性が高いため注目されています。ただ、感染症リスクが高まるため、コロナ渦では使いにくいという意見が医師の間でもあるようです(以下の動画参照)。
ジェンマブのパイプライン
2022年12月時点でのジェンマブのパイプラインは以下のとおりです。
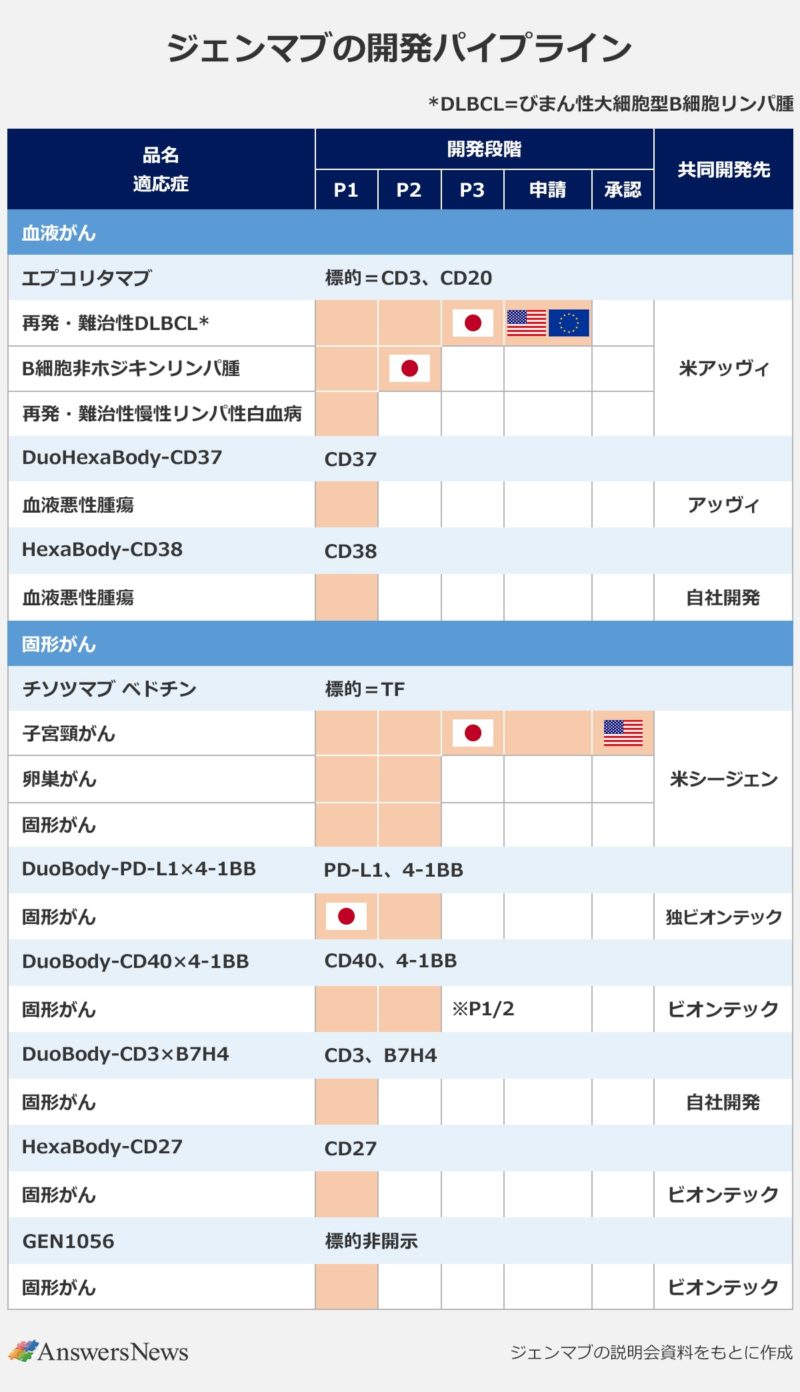
開発中のお薬で、注目したいのがEpcoritamab(エプコリタマブ)です。商品名は「(DuoBody ® -CD3xCD20」。アッヴィとの共同開発している再発・難治性びまん性大細胞型B細胞リンパ腫のお薬になります。
米国で2023年5月21日までに承認判断が下される予定になっています。欧州ではアッヴィが申請済み。欧州では、スイスのロシュが「Lunsumio」(一般名・mosunetuzumab)の承認取得済みです。
エプコリタマブは、米国で来年5月21日までに承認判断がある予定。欧州ではアッヴィが申請を済み。スイスのロシュが欧州で「Lunsumio」(一般名・mosunetuzumab)の承認を取得済み。
チソツマブベドチンは、米国では2021年に再発・転移性子宮頸がん治療薬「Tivdak」として迅速承認を取得しています。
多発性骨髄腫薬(ダラツムマブ)について
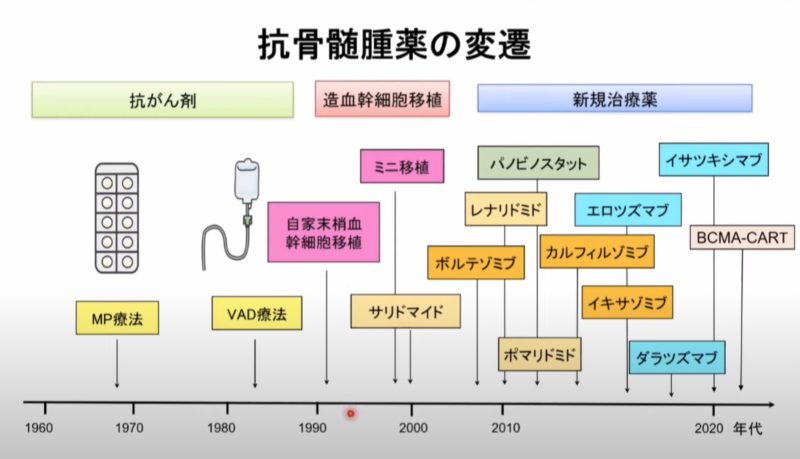
上図は多発性骨髄腫薬の変貌を年代順に表したものです(図1)。図の右側に記された「新規治療薬」領域のなかに「ダラツズマブ」とありますが、これがジェンマブが開発したお薬です。
日本においてダラツズマブは、17年に再発・難治性多発性骨髄腫に対して承認。2019年には初発の多発性骨髄腫に対して承認。2021年12月に保険適用されました。
- プロテアソーム阻害薬
総称名:ベルケイド<一般名:ボルテゾミブ(製薬会社:ヤンセンファーマ)>
総称名:カイプロリス<一般名:カルフィルゾミブ(製薬会社:小野薬品工業)>
総称名:ニンラーロ<一般名:イキサゾミブクエン酸エステル(製薬会社:武田薬品工業)> - 免疫調整薬
総称名:サレド<一般名:サリドマイド(製薬会社:藤本製薬)>
総称名:レブラミド<一般名:レナリドミド水和物(製薬会社:ブリストルマイヤーズ)>
総称名:ポマリスト<一般名:ポマリドミド(製薬会社:ブリストルマイヤーズ)> - モノクローナル抗体薬
総称名:ダラザレックス<一般名:ダラツムマブ(製薬会社:ヤンセンファーマ)>
総称名:ダラキューロ<一般名:ダラツムマブ(製薬会社:ヤンセンファーマ)>
総称名:サークリサ<一般名:イサツキシマブ(製薬会社:サノフィ)>
総称名:エムプリシティ<一般名:エロツズマブ(製薬会社:ブリストルマイヤーズ)>
血液がんフォーラム2022(Cancer Channel)から引用
上記3剤とステロイド剤を組み合わせた治療が、多発性骨髄腫の標準治療です。ダラザレックスもダラキューロもジェンマブが開発したお薬に違いはありません。違いは、ダラザレックスは点滴剤であるのに対して、ダラキューロは皮下注射になります。
ダラザレックスは何時間(初回7時間、2回目からは4時間)も点滴しなければなりませんが、ダラキューロであれば短時間で投与が可能であるため、ダラキューロが選ばれるようです。
売上高推移
さて、この銘柄にエントリーするかどうかは、今後のパイプライン承認状況によるかと思います。
ただ、過去の業績を振り返ると売上高が2021年に減少しているのが気になります。
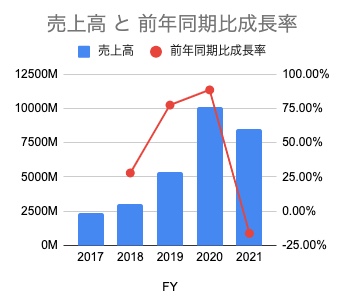
企業として何らかの問題を抱えて成長後退していたとしたら懸念材料になりますが、その心配はなさそうです。
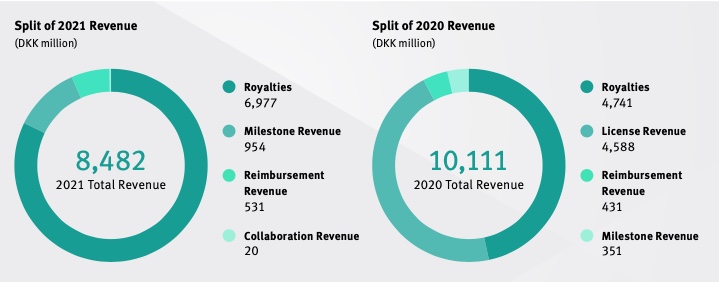
2020年に、アッヴィ社からライセンス収入として一時金4,398百万DKK(ライセンス売上高)が、計上されていたのが要因です(2021年年次決算資料から参照)。
2020年の売上高からアッヴィのライセンス収入4,398百万DKKを除いたとして、同年売上高は5,713百万DKKになります。
一時的ライセンス収入を除くと2019年から2021年の売上高成長率は以下のとおりになります。
2020年売上高:5,713百万DKK(前年同期比成長率+6.47%)
2021年売上高:8,482百万DKK(前年同期比成長率+48.5%)

そもそも、一時金を無かったことにして成長率をみるのはナンセンスかもしれませんが、これで投資する懸念材料はひとつ消えました。
ジェンマブ(GMAB)に関する2023年まとめ
2023/02/22:第4四半期決算 EPS、売上高ともにOK
Q4 FY22
EPS 予想$0.36 vs $0.13 ❌
売上高 予想$681M vs $744.06M ⭕️ YoY +86.4%
FY22
売上高 $2,094M YoY +72.0%
FY23 ガイダンス
売上高:DKK14,600~16,100M (2022:DKK14,595M)
YoY +5.5%
✅ FDAがpcoritamab を希少疾病用医薬品に指定
✅ 提携関係のアッヴィ社がepcoritamabのトップライン結果を発表
✅ epcoritamabの皮下投与は、米国と日本ではジェンマブ社、欧州ではアッヴィが申請
✅ epcoritamabの皮下投与生物製剤承認申請は米国FDA優先審査の対象になった
✅epcoritamabの再発・難治性びまん性大細胞型B細胞リンパ腫患者に対する販売許可申請が欧州医薬品庁で有効化
✅ 2022年、セーゲン社と共同開発中のTivdakが初めて通年で使用可能になった
✅ ヤンセンのTECVAYLI(teclistamab)が、DuoBodyを用いた医薬品として2番目の薬事承認を取得
ジェンマブ(GMAB)に関する2022年まとめ
2022/12/23:IBD、バイオ銘柄トップ5にリストアップ
2022/12/12:日本参入を本格始動

2022/11/09:9月決算発表 EPS、売上高、ガイダンスすべてOK
9月 FY22
EPS 予想$0.23 vs $0.53 ⭕️
売上高 予想$473.493M vs $551.031M⭕️
YoY +54.0%
2022年ガイダンス
売上高 12,000-13,000→13,500-14,500DKK M に上方修正
✅ダラザレックスの売上高は前年同期比+35%成長
✅ロイヤリティ収入は前年同期比+75%成長
✅再発・難治性びまん性大細胞型B細胞リンパ腫薬「Epcoritamab(エプコリタマブ)」において重要なアップデートが2点あり。2022年下半期に米国食品医薬品局 (US FDA) に生物学的製剤承認申請 (BLA) 。アッヴィは、全身療法を2ライン以上行った再発・難治性のびまん性大細胞型B細胞リンパ腫(DLBCL)患者さんの治療薬として、epcoritamabのSC版を欧州医薬品庁(EMA)に販売許可申請し、EMAにより有効性が確認されました。



コメント